|
Решебник по Химии. 8 класс. Габриелян. Рабочая тетрадь
|
|
| Alicerok | Дата: Среда, 07.10.2015, 11:11 | Сообщение # 61 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
|
Тема 31. Реакции замещения.
Часть I
1. Признаки реакций замещения:
- вступают в реакцию два вещества – простые и сложные;
- образуются в результате реакции также два вещества – новое простое и новое сложное.
2. Два правила ряда активности металлов:

-металлы, стоящие в ряду активности до H2, вытесняют его из растворов кислот;
- металлы, стоящие в ряду активности до металла соли, вытесняют его из растворов солей.
|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 11:20 | Сообщение # 62 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Часть II
1. Запишите уравнения реакций замещения.
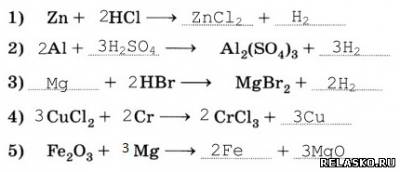
2. Запишите уравнения возможных реакций.
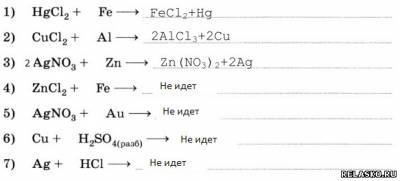
3. Напишите уравнения реакций замещения:

4. Допишите уравнение реакции

Дайте характеристику записанной реакции по следующим признакам:
1) число и состав исходных веществ и продуктов реакции – замещение;
2) тепловой эффект – экзотермическая;
3) направление протекания – необратимая;
4) участие катализатора – некаталитическая.
5. 39 г технического цинка, содержащего 20% примесей, растворили в избытке соляной кислоты. Найдите объём полученного водорода (н. у.) и количество вещества соли.

6. Железо массой 1,12 г полностью прореагировало с раствором сульфата меди (II). Найдите массу образовавшегося осадка меди. Какое количество вещества сульфата железа (III) при этом получилось?

7. Придумайте рисунки «Взаимодействие различных металлов с соляной кислотой» и «Взаимодействие различных кислот с цинком», иллюстрирующие зависимость скорости протекания реакций от природы металла и кислоты.
|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 11:22 | Сообщение # 63 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Тема 32. Реакции обмена.
Часть I
1. Признаки реакций обмена:
- вступают в реакцию два сложных вещества;
- образуются в результате реакции два новых сложных вещества.
2. Условия протекания реакции обмена до конца:
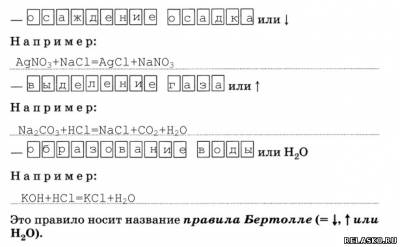
3. Частный случай реакций обмена – это реакция между щёлочью и кислотой, которая носит название реакции нейтрализации.
Например: NaOH+HCl=NaCl+H2O
|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 11:25 | Сообщение # 64 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Часть II
1. Запишите уравнения реакций обмена между:

2. Составьте уравнения реакций, идущих до конца.
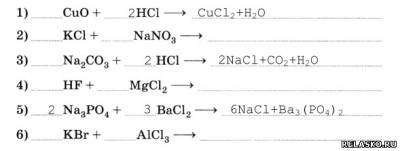
3. Напишите уравнения реакций обмена, протекающих:

4. Установите соответствие между типом и уравнением химической реакции.
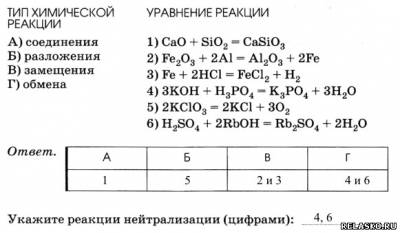
5. Определите массу соли и количество вещества воды, полученных при взаимодействии гидроксида меди (II) с 58,8 г серной кислоты.

6. Запишите уравнения реакций со следующими продуктами:

7. Запишите уравнения 3-4 реакций обмена, в результате которых образуется сульфат железа (II).

|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 11:28 | Сообщение # 65 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Тема 33. Типы химических реакций на примере свойств воды.
Часть I
1. Реакции разложения воды:
- под действием электрического тока называют электролизом;
- под действием света называют фотолизом.
Уравнение реакции: 2Н2О = 2Н2 + О2
2. Реакции соединения воды с оксидами:
металлов идут с образованием щелочей, например:
неметаллов идут с образованием кислоты, например: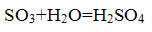
3. Реакции замещения водорода в молекуле воды на металл идут с образованием щёлочи:
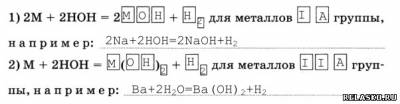
4. Реакции обмена — это реакции разложения веществ водой, или реакции гидролиза, например:

|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 11:33 | Сообщение # 66 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Часть II
1. «Химическим антонимом» реакции разложения воды является её синтез из соответствующих простых веществ. Напишите уравнение этого процесса:
2Н2 + О2=2Н2О
Придумайте и решите задачу, если известен объём одного из исходных веществ (н. у.), а требуется найти массу воды.
При взаимодействии 11,2 л углекислого газа с гидроксидом натрия, образовались соль и вода. Найти массу воды.

2. Запишите уравнения возможных реакций соединения с водой:
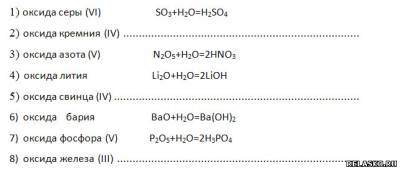
Распределите образовавшиеся гидроксиды на две группы.

3. Запишите уравнения реакций замещения с водой:

4. Запишите уравнения реакций гидролиза:

5. Запишите название продуктов гидролиза органических веществ, используя свои знания по теме «Пищеварительная система» из курса биологии.
1) Белки + вода→аминокислота.
2) Крахмал + вода→глюкоза.
3) Жиры + вода→глицерин + оксокислота.
6. Найдите массу фосфорной кислоты, которая образуется при растворении в воде 2,5 моль оксида фосфора (V).

7. Найдите массу щёлочи, которая образуется при растворении в воде 1,5 моль натрия.

|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 11:43 | Сообщение # 67 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Тема 34. Растворы. Растворение.
Часть I
1. Растворы — это гомогенные смеси, состоящие из 2 или более однородных частей, то есть частиц растворённого вещества, растворителя и продуктов их взаимодействия.
2. Две точки зрения на растворы и растворение.
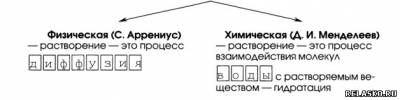
3. Гидратация — это взаимодействие молекул вещества с водой.
Кристаллогидраты — это соли, в состав которых входит вода.
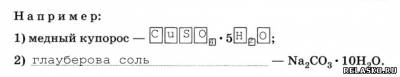
4. Различают растворы
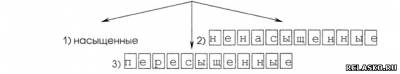
Дайте определение каждого типа растворов.
1) раствор, в котором при данной температуре вещество больше не растворяется.
2) раствор, в котором при данной температуре меньше раств. вещества, чем в насыщенном.
3) раствор, в котором больше вещества, чем в насыщенном.
|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 11:50 | Сообщение # 68 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Часть II
1. Подпишите схему «Значение растворов».
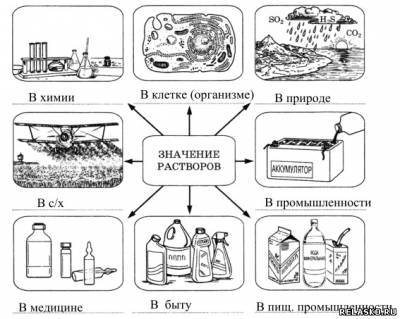
2. Заполните таблицу «Теории растворов».
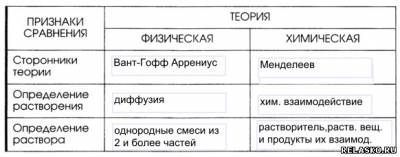
3. Сформулируйте основные положения физико-химической теории растворов, которая принята в настоящее время.
1) При добавлении соли в воду происходит процесс химического взаимодействия.
2) В растворе одновременно находятся и растворённое вещество, и растворитель, и продукты их взаимодействия.
3) Растворение также процесс, в результате которого имеют место и тепловые явления.
4. Составьте формулы кристаллогидратов.

5. Заполните текст формулами и названиями соединений, числовыми значениями.
Примечание. Воспользуйтесь данными графиков растворимости веществ (см. рис. 126 в учебнике) и таблицей растворимости.

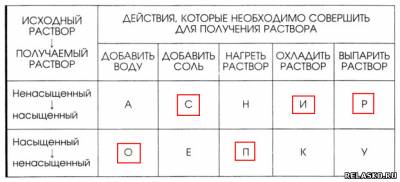
6. Установите соответствие между действием, которое нужно совершить для получения раствора, и типом раствора. Из букв, соответствующих правильным ответам, вы составите название раствора сахара в воде: сироп.
7. Растворимость хлорида калия в воде при 60 °С равна 50 г. Определите массовую долю соли в растворе, насыщенном при указанной температуре.

8. По графику (см. рис. 126 в учебнике) определите растворимость сульфата калия при 80 °С. Рассчитайте массовую долю соли в растворе, насыщенном при указанной температуре.

9. Навеску 161 г глауберовой соли Na2S04 • ЮН20 растворили в 180 л воды. Вычислите массовую долю сульфата натрия в полученном растворе. Сколько ионов каждого вида в нём находится?

10. Заполните таблицу «Научные достижения Д. И. Менделеева и С. Аррениуса».

|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 12:27 | Сообщение # 69 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Тема 35. Основные положения теории электролитической диссоциации (ТЭД).
Часть I
1. Электролиты — это вещества, проводящие электрический ток.
Признаки электролитов:
- состоят из ионов;
- растворяются в воде.
2. Диссоциация – это процесс распада электролита на ионы.
3. Основные положения ТЭД.

|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 12:30 | Сообщение # 70 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Часть II
1. При испытании веществ на электропроводность лампочка загорится, если погрузить электроды:
2) в водный раствор гидроксида калия
Напишите уравнение реакции диссоциации электролита.
КОН = К+ + ОН-
2. Наиболее сильным электролитом является:
1) фтороводородная кислота
Напишите уравнение реакции диссоциации наиболее сильного электролита.
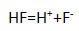
3. К слабым электролитам относится каждое из веществ:
2) сероводородная кислота и гидрат аммиака
Напишите уравнения реакции диссоциации наиболее сильных электролитов.
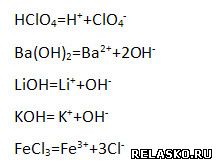
4. Степень электролитической диссоциации уксусной кислоты в растворе уменьшится:
4) при добавлении щёлочи
5. Наибольшее (суммарное) число ионов образуется при диссоциации 1 моль:
3) сульфата железа (III)
Напишите уравнения электролитической диссоциации.

6. Наибольшее число ионов натрия образуется при диссоциации 1 моль:
4) фосфата натрия
Напишите уравнения электролитической диссоциации.
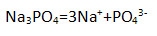
7. Установите соответствие между названием соли и образующимися в результате диссоциации анионами.

|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 12:33 | Сообщение # 71 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Тема 36. Оксиды, их классификация и химические свойства.
Часть I
1. Оксиды – это бинарные соединения атомов элементов с кислородом, в которых кислород проявляет степень окисления минус 2.
2. Классификация оксидов
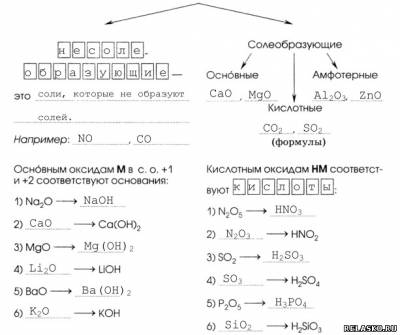
3. Химические свойства основных и кислотных оксидов.
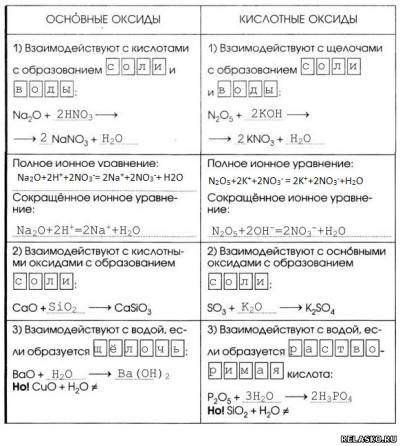
|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 12:36 | Сообщение # 72 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Часть II
1. Основание образуется при взаимодействии с водой оксида, формула которого:
3) СаО
Запишите уравнение реакции.
CaO+H2O=Ca(OH)2
2. С гидроксидом натрия реагирует:
3) SiO2
4) P2O5
Составьте уравнения возможных реакций

3. С соляной кислотой реагирует:
1) оксид железа (III)
4) оксид меди (II)
Составьте уравнения возможных реакций

4. Запишите по одному уравнению реакций соединения и разложения для получения:
1) оксида меди (II)
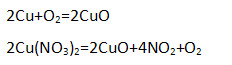
2) оксида кремния (IV)

5. Какой объём сернистого газа (н. у.) образуется при сгорании 67,2 л сероводорода?

6. Сколько граммов 25%-го раствора гидроксида натрия потребуется для поглощения объёма сернистого газа, найденного при решении задачи 5?

|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 12:38 | Сообщение # 73 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Тема 37. Кислоты, их классификация и химические свойства в свете ТЭД.
Часть I
1. Кислоты — это электролиты, которые при диссоциации образуют в качестве катионов только катионы водорода.
2. Вспомните классификацию кислот и распределите кремниевую, соляную, азотную, угольную, фосфорную кислоты в соответствующие группы, вписав их формулы.

3. Общие химические свойства кислот.

4. Приведите примеры уравнений реакций, характеризующих общие свойства кислот, в молекулярном, полном ионном и сокращённом ионном видах:

|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 12:40 | Сообщение # 74 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Часть II
1. Соляная кислота взаимодействует со следующими из перечисленных веществ:
медь, магний, оксид меди (II), оксид кремния (IV), сульфат калия, нитрат серебра, карбонат кальция.

2. Приведите не менее трёх молекулярных уравнений, соответствующих следующему сокращённому ионному:

3. Приведите не менее трёх молекулярных уравнений, соответствующих следующему сокращённому ионному:

4. Приведите не менее трёх молекулярных уравнений, соответствующих следующему сокращённому ионному:
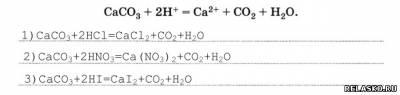
5. Определите неизвестные вещества и запишите молекулярные и ионные уравнения реакций, протекающих согласно схеме:
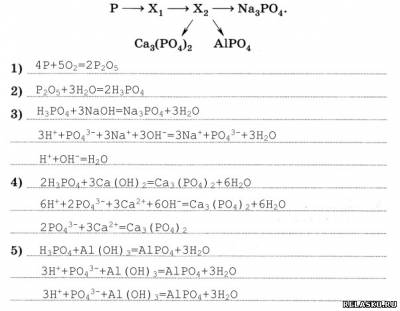
6. Сколько граммов 30%-й азотной кислоты потребуется для взаимодействия с 250 г известняка, содержащего 20% примесей? Какой объём углекислого газа (н. у.) при этом образуется?

|
| |
| |
| Alicerok | Дата: Среда, 07.10.2015, 12:43 | Сообщение # 75 |
|
Майор
Группа: Проверенные
Сообщений: 88
Награды: 0
Репутация: 0
Статус: Offline
| Тема 38. Основания, их классификация и химические свойства в свете ТЭД.
Часть I
1. Основания — это электролиты, которые при диссоциации образуют в качестве анионов только гидроксид ионы.
2. Вспомните классификацию оснований и распределите гидроксид натрия, гидроксид магния, гидроксид кальция, гидрат аммиака по соответствующим группам, вписав их формулы.
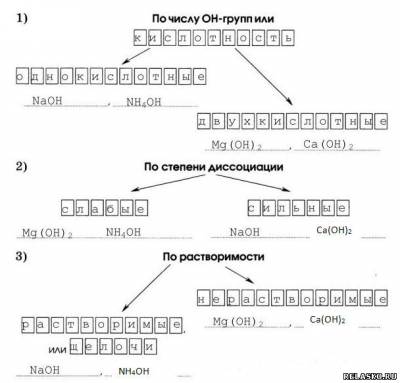
3. Общие химические свойства оснований.
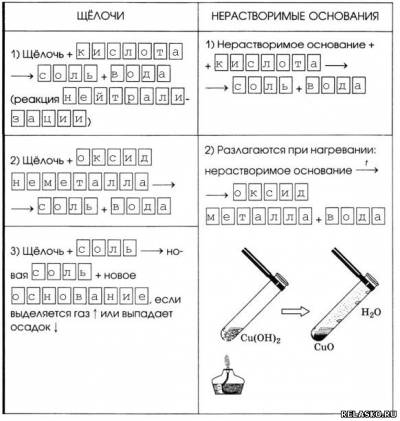
4. Приведите примеры уравнений реакций, характеризующих общие свойства оснований, в молекулярном, полном ионном и сокращённом ионном видах.

Смотреть решебник далее...
|
| |
| |