|
Решебник по Химии. 8 класс. Габриелян. Рабочая тетрадь
|
|
| Alicerok | | Сообщение # 16 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
|
Тема 8. Ионная химическая связь.
Часть I
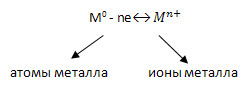
1. Атомы металлов, отдавая внешние электроны, превращаются в положительные ионы:

где n — число электронов внешнего слоя атома, соответствующее номеру группы химического элемента.
2. Атомы неметаллов, принимая электроны, недостающие до завершения внешнего электронного слоя, превращаются в отрицательные ионы:
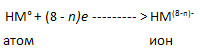
3. Между разноимённо заряженными ионами возникает связь, которая называется ионной.
4. Дополните таблицу «Ионная связь».

|
| |
| |
| Alicerok | | Сообщение # 17 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Дополните схемы образования положительно заряженных ионов. Из букв, соответствующих правильным ответам, вы составите название одного из древнейших природных красителей: индиго.

2. Поиграйте в «крестики-нолики». Покажите выигрышный путь, который составляют формулы веществ с ионной химической связью.
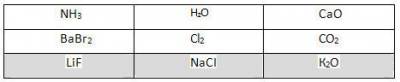
3. Верны ли следующие утверждения?

3) верно только Б
4. Подчеркните пары химических элементов, между которыми образуется ионная химическая связь.
1) калий и кислород
3) алюминий и фтор
Составьте схемы образования химической связи между выбранными элементами.
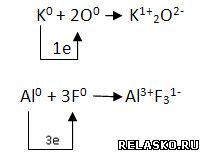
5. Придумайте рисунок в стиле комиксов, отражающий процесс образования ионной химической связи.
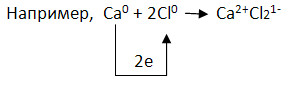
6. Составьте схему образования двух химических соединений с ионной связью по условной записи:
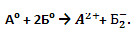
Выберите химические элементы «А» и «Б» из следующего списка:
кальций, хлор, калий, кислород, азот, алюминий, магний, углерод, бром.
Подходят для данной схемы кальций и хлор, магний и хлор, кальций и бром, магний и бром.
7. Напишите небольшое литературное произведение (эссе, новеллу или стихотворение) об одном из веществ с ионной связью, которое человек применяет в быту или на производстве. Для выполнения задания используйте возможности Интернета.
Хлорид натрия – вещество с ионной связью, без него нет жизни, хотя, когда его много – это тоже нехорошо. Даже есть такая народная сказка, где рассказывается о том, что принцесса любила своего отца короля так сильно, как соль, за что была изгнана из королевства. Но, когда король однажды попробовал еду без соли и понял, что есть невозможно, он тогда понял, что дочь его очень сильно любила. Значит, соль – есть жизнь, но её потребление должно быть в
меру. Потому что чрезмерное потребление соли сильно вредит здоровью. Избыток соли в организме приводит к заболеванию почек, меняет цвет кожи, задерживает излишнюю жидкость в организме, что приводит к отёкам и нагрузке на сердце. Поэтому, надо контролировать потребление соли. 0,9% раствор хлорида натрия – это физиологический раствор, используется для вливания лекарств в организм. Поэтому, очень трудно ответить на вопрос: полезна или вредна соль? Она нам нужна в меру.
|
| |
| |
| Alicerok | | Сообщение # 18 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 9. Ковалентная химическая связь.
Часть I
1. Связь между атомами элементов – неметаллов за счёт образования общих электронных пар называется ковалентной или атомной.
2.
3. По числу общих электронных пар между атомами различают (приведите примеры):
1) одинарная связь Н₂, Cl₂
2) двойная связь CO₂, NO
3) тройная связь C₂H₂, N₂
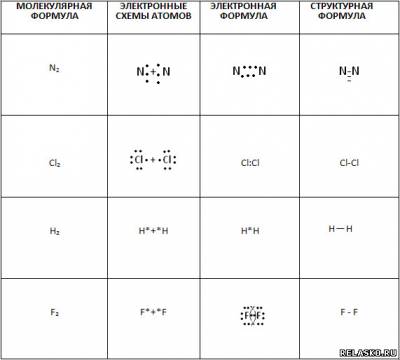
4. Дополните таблицу «Ковалентная связь».
|
| |
| |
| Alicerok | | Сообщение # 19 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Поиграйте в «крестики-нолики». Покажите выигрышный путь, состоящий из формул веществ с ковалентной связью, и запишите схемы их образования.
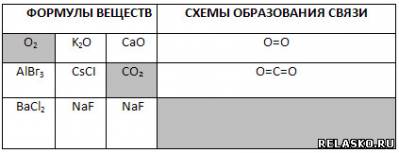
2. Выберите формулы соединений с ковалентной химической связью. Из букв, соответствующих правильным ответам, составьте название химического элемента, который входит в состав черного пороха: сера.
3) Вг2 С
5) Р4 Е
7) О3 Р
9) S2 А
3. Постройте график зависимости кратности химической связи от её длины. Сделайте вывод:
Кратность химической связи обратно пропорциональна длине.
4. Постройте график зависимости прочности химической связи от её кратности. Сделайте вывод:
Прочность химической связи прямо пропорциональна кратности.
5. Придумайте рисунок в стиле комиксов, отражающий процесс образования ковалентной неполярной химической связи.
|
| |
| |
| Alicerok | | Сообщение # 20 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 10. Ковалентная полярная химическая связь.
Часть I
1. Электроотрицательность (ЭО) — это способность атомов оттягивать к себе электронные пары.
2.
3. Если ковалентная химическая связь образуется между атомами разных элементов-неметаллов, то общие электронные пары смещены в сторону более электроотрицательного элемента. На нём возникает избыточный отрицательный заряд, а на атоме-партнёре — избыточный положительный заряд. Такая связь называется ковалентной полярной.

4. 
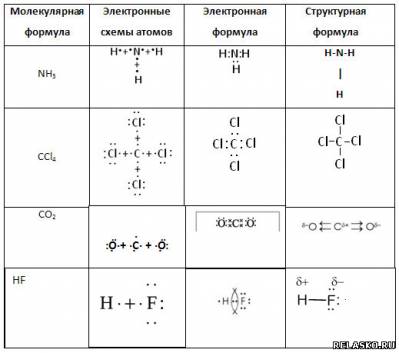
5. Дополните таблицу «Ковалентная полярная связь».
|
| |
| |
| Alicerok | | Сообщение # 21 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Поиграйте в «крестики-нолики». Покажите выигрышный путь, состоящий из формул веществ с ковалентной полярной связью, и запишите схемы их образования.
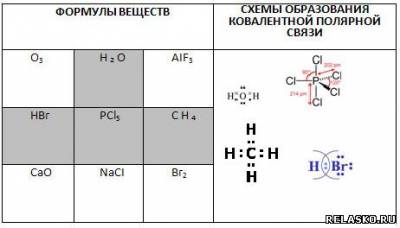
2. Выберите формулы соединений с ковалентной полярной химической связью. Из букв, соответствующих правильным ответам, вы составите слово, означающее имитацию алмаза или другого драгоценного камня, выполненного из стекла: страз.
1) HF С
3) FeBr3 Т
5) SO2 Р
7) CO2 А
9) PCl5 З
3. Постройте график зависимости порядкового номера химического элемента от электроотрицательности элементов одного периода. Точные значения электроотрицательности найдите с помощью Интернета.
Сделайте вывод:
С увеличением порядкового номера ЭО растёт.
4. Постройте график зависимости порядкового номера химического элемента от электроотрицательности элементов одной главной подгруппы.
Точные значения электроотрицатель¬ности найдите с помощью Интернета.
В группе с увеличением порядкового номера ЭО уменьшается.
5. Наиболее полярной является химическая связь в молекуле:
4) фтороводорода — HF
6. Расположите следующие вещества в порядке уменьшения полярности химической связи.
4) фосфид калия — К3Р
2) фосфид алюминия — АlР
3) хлорид фосфора (V) — РСl5
1) белый фосфор — Р4
|
| |
| |
| Alicerok | | Сообщение # 22 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 11. Металлическая химическая связь. Обобщение знаний о типах химической связи.
Часть I
1. Связь между атом-ионами в металлах и сплавах за счёт обобществлённых внешних электронов называется металлической.
2. Схема образования металлической связи:
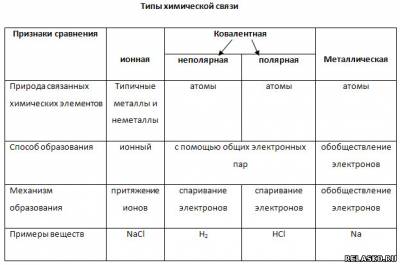
3. Заполните таблицу «Типы химической связи».
|
| |
| |
| Alicerok | | Сообщение # 23 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Установите соответствие между типом химической связи и формулами веществ. Из букв, соответствующих правильным ответам, вы составите название первого металлического сплава, который использовал человек: бронза.
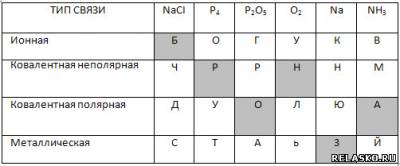
2. Из ряда формул веществ:
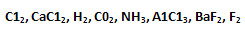
- выберите те, которые соответствуют электронной формуле вещества, представленной в общем виде.
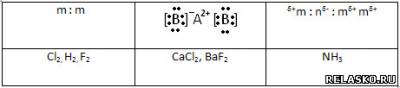
3. Напишите формулы веществ, образованных элементами 2-го периода с помощью всех типов химической связи.
Запишите схемы образования веществ с ионной и ковалентной полярной химической связью.

4. Исключите «лишнее».
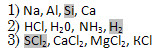
5. Верны ли следующие утверждения?
А. Природа любой химической связи электростатическая.
Б. В одном веществе может быть только один вид химической связи.
4) оба суждения неверны
6. Между атомами элементов с порядковыми номерами 11 и 9 образуется химическая связь:
1) ионная
7. Верны ли следующие суждения?
А. Химический элемент кальций образует вещества, в которых наблюдаются все типы химических связей.
Б. Вещество кальций Са и нитрид кальция Ca3N2 образованы соответственно с помощью металлической и ковалентной неполярной связей.
4) оба суждения неверны
|
| |
| |
| Alicerok | | Сообщение # 24 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 12. Простые вещества. Простые вещества — металлы.
Часть I
1. Металлы (М) располагаются в I-III группах, или в нижней части IV-VI групп. Только из металлов состоят В группы.
2. У атомов металлов 1—3 электрона во внешнем электронном слое и сравнительно большой радиус атома. Атомы металлов имеют тенденцию к отдаче внешних электронов.
3. Простые вещества — металлы состоят из элементов, связанных металлической химической связью, которую можно отобразить общей схемой:

4. Все М — твёрдые вещества, кроме Hg . Самые мягкие металлы IA группы, самый твердый —Cr.
5. М обладают тепло- и электропроводностью и имеют металлический блеск.
6.Олово обладает свойством образовывать два простых вещества - белое и серое, т. е. свойством аллотропии.
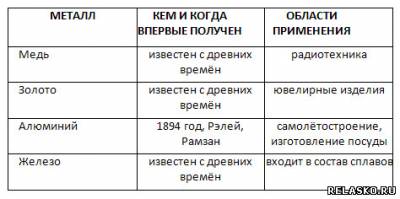
7. Дополните таблицу "Свойства и применение некоторых металлов".
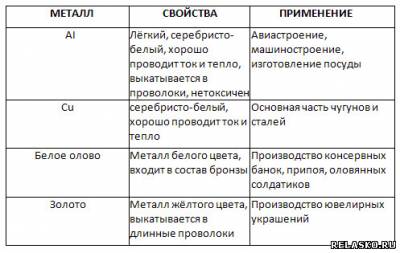
|
| |
| |
| Alicerok | | Сообщение # 25 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Выберите названия простых веществ — металлов. Из букв, соответствующих правильным ответам, вы составите название металла, которое в переводе с греческого означает «камень»: литий.
2) магний Л
3) кальций И
5) медь Т
7) золото И
8) ртуть Й
2. Неверны следующие утверждения, характеризующие металлы:
5) непластичные и нековкие
3. Выберите четыре самых электропроводных металла (цифры расположите в порядке убывания электропроводности) из перечня:
1) серебро
2) золото
3) алюминий
4) железо
5) марганец
6) калий
7) натрий
Ответ: 1, 2, 3, 7.
4. Составьте схемы образования металлической химической связи для веществ с формулами:
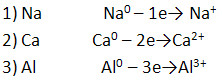
5. Проанализируйте рисунок «Металлическая кристаллическая решётка».
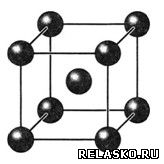
Сделайте вывод о причинах пластичности, тепло- и электропроводности металлов.
Каждый атом металла окружен восемью соседними атомами. Оторвавшиеся внешние электроны свободно движутся от одного образовавшегося иона к другому, соединяя ионный остов металла в гигантскую молекулу. Высокая теплопроводность, электрическая проводимость металлов обусловлены наличием в их кристаллических решетках подвижных электронов, перемещающихся под действием электрического поля. Большинство металлов пластичны из-за смещения слоев атомов металлов без разрыва связи между ними.
6. Заполните таблицу «Металлы». Данные для таблицы найдите с помощью дополнительных источников информации, в том числе Интернета.
7. С помощью Интернета и других источников информации подготовьте небольшое сообщение на тему «Ртуть в жизни человека» по следующему плану:
1) знания о ртути в древности и в Средние века;
2) токсичность ртути и меры безопасности при работе с ней;
3) применение ртути в современной промышленности.
1) Ртуть входила в число 7 металлов, её считают прародительницей всех металлов, использовали не только саму ртуть, но и её сплав киноварь.
2) Она очень токсична, испаряется при комнатной температуре, и при вдыхании отравляет человека. Накапливаясь в организме, она поражает внутренние органы, дыхательные пути, кроветворные органы и головной мозг.
3) Ртуть используют очень широко. В химической промышленности в качестве катода при получении гидроксида натрия, как катализатор при получении многих органических соединений, при растворении урановых блоков (в атомной энергетике). Этот элемент применяется при изготовлении ламп дневного света, кварцевых ламп, манометров, термометров и других научных приборов.
|
| |
| |
| Alicerok | | Сообщение # 26 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 13. Простые вещества — неметаллы.
Часть I
1. Неметаллы (НМ) располагаются в III-VII группах.
Только из НМ состоит группа галогенов. По физическим свойствам к НМ следует отнести также VIIIА группу, или группу благородных газов.
2. У атомов неметаллов 4 и более электрона во внешнем слое, небольшой радиус атома, например С, у атома которого 4 внешних е. Поэтому атомы НМ стремятся довести недостающие до 8е. Это свойство атомов характеризуется электроотрицательностью. В соответствии с ним НМ образуют особый ряд:
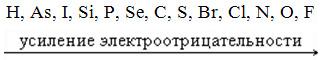
3. Молекулы простых веществ НМ образованы за счёт ковалентной неполярной связи. Двухатомные молекулы имеют, например, следующие простые вещества: О₂, Сl₂, N₂, галогены;
трехатомная молекула О₃ - у озона.
4. Аллотропия для неметаллов более характерна, чем для металлов.
Заполните таблицу «Аллотропные модификации неметаллов» . Данные для таблицы найдите с помощью дополнительных источников информации, в том числе Интернета.
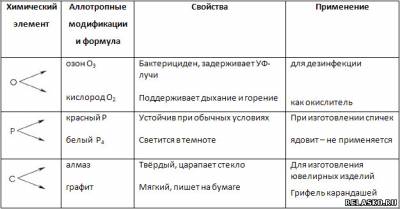
5. Заполните таблицу «Сравнение свойств металлов и неметаллов».
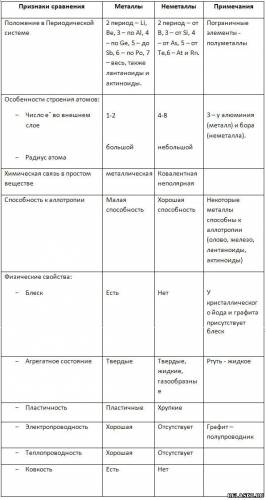
|
| |
| |
| Alicerok | | Сообщение # 27 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Выберите названия простых веществ — неметаллов. Из букв, соответствующих правильным ответам, вы составите название неметалла, которое в переводе с греческого означает «гибель, разрушение»: фтор.
1) бром Ф
2) магний Т
6) неон О
8) йод Р
2. Распределите вещества Na, Br2, Ne, I2, Li, Не, Сl2 на три группы. Вычислите и запишите относительные молекулярные массы галогенов.
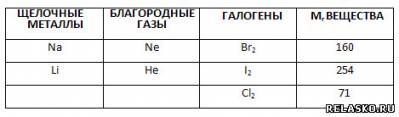
3. Неверны следующие утверждения, характеризующие неметаллы:
2) при обычных условиях фтор, хлор и бром — газы.
4) атомы этих элементов стремятся отдать электроны с внешнего энергетического слоя.
4. Установите соответствие между названием вещества и его свойствами.

А – 1,3,6
Б – 2,4,5
5. Заполните таблицу «Неметаллы». Данные для таблицы найдите с помощью дополнительных источников информации, в том числе Интернета.
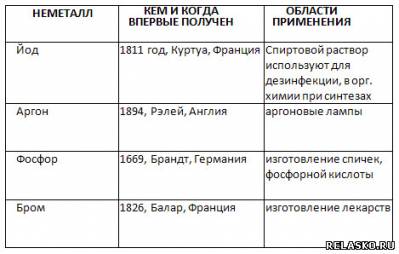
6. Расположите следующие простые вещества — неметаллы в порядке возрастания их плотности.
6) кремний
7) красный фосфор
1) йод
2) бром
4) хлор
3) азот
5) водород
7. Расположите следующие простые вещества — неметаллы в порядке возрастания интенсивности их окраски.
6) йод
4) бром
1) хлор
3) озон
2) кислород
5) азот
|
| |
| |
| Alicerok | | Сообщение # 28 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 14. Количество вещества. Молярная масса.
Часть I
1. Единицей количества вещества является моль. Обозначается n или ню.
2. Моль — это также количество вещества, в котором содержится 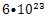 молекул или частиц вещества. Это число называется числом Авогадро и обозначается Nа. молекул или частиц вещества. Это число называется числом Авогадро и обозначается Nа.
3. Чтобы отмерить вещество количеством в 1 моль, нужно взять столько граммов этого вещества, какова его Mr или Ar.
4. Масса 1 моль вещества называется молярной массой — M. Она измеряется в г/моль и численно равна Mr вещества.
5. Количество вещества — это величина, равная отношению массы вещества к его молярной массе:
n = m/M => m = n• M.
6. Число частиц вещества равно произведению числа Авогадро на количество вещества:
N = n •Na => n = N/Na.
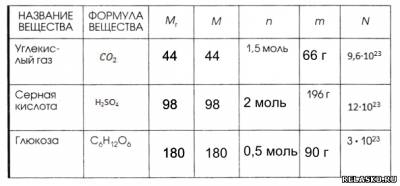
7. Дополните таблицу, делая необходимые вычисления.
Сообщение отредактировал Alicerok - Вторник, 06.10.2015, 16:41 |
| |
| |
| Alicerok | | Сообщение # 29 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Впишите пропущенные числа.
1) Ar(Na)=23 => 23 г натрия содержат 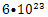 атомов Na. атомов Na.
2) Мг(02)=32 => 32 г кислорода содержат 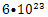 молекул 02. молекул 02.
3) Мг (СО) = 28 => 28 г угарного газа содержат 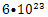 молекул СО. молекул СО.
2. Установите соответствие между названием величины и её условным обозначением.
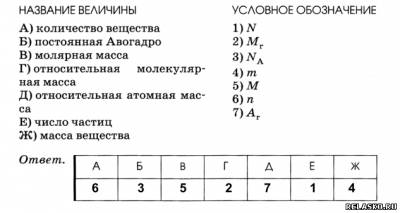
3. Впишите пропущенные названия веществ, частиц вещества, числа и единицы измерения.
1) 1 моль вещества Н2 содержит 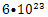 молекул. молекул.
2) 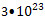 молекул углекислого газа С02 составляют количество вещества, равное 0,5 моль. молекул углекислого газа С02 составляют количество вещества, равное 0,5 моль.
3) 64 г вещества О2 составляют количество вещества, равное 2 моль.
4) 0,5 моль серной кислоты H2S04 составляют массу вещества, равную 49 г.
4. Запишите формулу, по которой можно рассчитать молярную массу вещества, если известно его количество и масса.
М = m•N
5. Запишите формулу, по которой можно рассчитать массу вещества, если известно число структурных частиц данного вещества.
m = N•M/Na
6. Какие величины можно рассчитать, если известно количество вещества?
Массу, число частиц.
7. Сколько молекул содержится в 180 г воды? Решите задачу двумя способами.

8. Придумайте условие задачи, используя величины из задания 2. Найти массу воды химическим количеством 10 моль. Решите её любым способом.
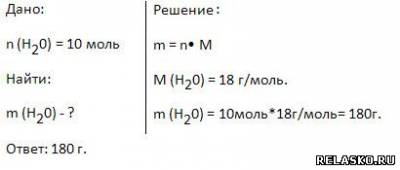
|
| |
| |
| Alicerok | | Сообщение # 30 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 15. Молярный объём газов.
Часть I
1. 1 моль любого газа при н. у. занимает одинаковый объём, равный 22,4 л. Этот объём называется молярный и обозначается Vm.
2. Количество вещества (n) — отношение объёма газа при н. у. к молярному объёму:
n = V/Vm=> Vm измеряется в л/моль.
3. Следовательно, количество вещества
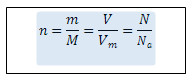
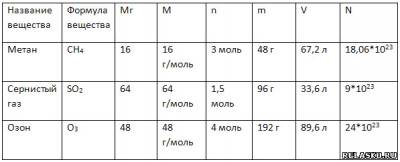
4. Дополните таблицу «Количественные характеристики веществ», делая необходимые вычисления.
Смотреть решебник далее...
|
| |
| |