|
Решебник по Химии. 8 класс. Габриелян. Рабочая тетрадь
|
|
| Alicerok | | Сообщение # 46 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
|
Часть II
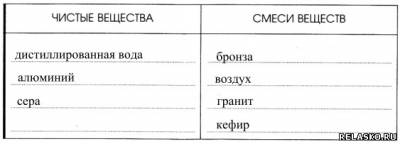
1. Распределите по двум столбцам следующие вещества:
дистиллированная вода, бронза, алюминий, воздух, гранит, кефир, сера.
2. Напишите, какие минералы входят в состав горной породы – гранита.
Кремнезем, полевой шпат, кварц, плагиоклаз.
3. Приведите состав двух используемых на кухне смесей, изучив сведения на их упаковках.
1) поваренная соль
2) сахар
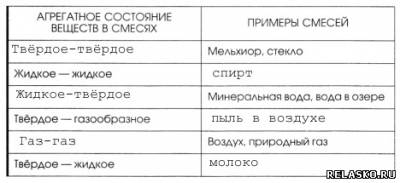
4. Дополните таблицу, записав в неё по два примера смесей.
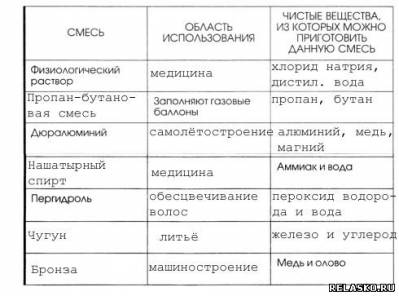
5. Дополните таблицу «Смеси и их применение». Для выполнения задания используйте возможности Интернета
6. Подготовьте сообщение или презентацию на тему «Использование химического анализа в той или иной области человеческой деятельности» (область применения выберите самостоятельно). Для выполнения задания используйте возможности Интернета.
Определение нитратов в пищевых продуктах с целью обеспечения безопасности и качества, в частности, овощей и фруктов.
Каждый крупный рынок, где продают овощи и фрукты имеет химическую лабораторию, в которой проводят анализ – определяют количество нитрат – ионов в образцах. Предельно допустимое количество нитратов в овощах нормируется нормативными документами – ГОСТами, СанПинами, где для каждого вида продукции указана предельная допустимая концентрация нитрат-ионов. Если содержание нитратов в данном образце превышает эту норму, то продукцию бракуют и не допускают к продаже.
Анализ проводится следующим способом.
Образец данного овоща тщательно моется, измельчается, берётся навеска, равная 10 граммам и к ней добавляются алюмокалиевые квасцы. Специальный прибор – нитратомер – определяет в этом образце содержание нитратов.
|
| |
| |
| Alicerok | | Сообщение # 47 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 24. Массовая и объёмная доли компонентов смеси.
Часть I
1. Для жидких и твёрдых смесей массовая доля компонента (w) рассчитывается по формуле:

2. Объёмная доля компонента газообразной смеси (φ) рассчитывается по формуле:

3. Используя материал пунктов 1 и 2, выведите формулы для расчётов:

4. Для расчёта m раствора, если известны его плотность и объём, используют формулу, известную из курса физики: m(р-ра)=V*P
|
| |
| |
| Alicerok | | Сообщение # 48 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. В 40 г дистиллированной воды растворили 2 г хлорида натрия. Рассчитайте массовую долю соли в полученном растворе.

2. В 2 л раствора серной кислоты содержится 456 г H2SO4. Рассчитайте массовую долю растворённого вещества, учитывая, что плотность раствора равна 1,14 г/мл.

3. Сколько воды и соли нужно взять, чтобы приготовить 250 г 10%-го раствора нитрата натрия?

4. К 1 кг 60%-го раствора соли добавили 50 г этой соли. Какова массовая доля соли в полученном растворе? Ответ округлить до десятых.

5. Какова массовая доля сахара в растворе, полученном при упаривании 200 г 20%-го раствора до 70 г? Ответ округлить до десятых.

6. Смешали 120 г 40%-го и 280 г 10%-го раствора азотной кислоты. Определите массовую долю азотной кислоты в полученном растворе.

7. Сколько хлороводорода нужно растворить в 1 м3 воды, чтобы получить 20%-й раствор? Вычислите массу и объём (н. у.) хлороводорода.

8. В воздухе содержится 21% кислорода и 78% азота по объёму. Рассчитайте объём кислорода и азота в 250 м3 воздуха. Определите для каждого газа количество вещества и массу.

9. К 300 л воздуха добавили 60 л азота. Вычислите массы кислорода и азота, которые можно получить из этой смеси.

|
| |
| |
| Alicerok | | Сообщение # 49 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 25. Изменения, происходящие с веществами.
Часть I
1. Для получения чистых веществ из жидких или гетерогенных смесей используют различные химические свойства веществ, образующих данные смеси.
2. Способы разделения смесей.
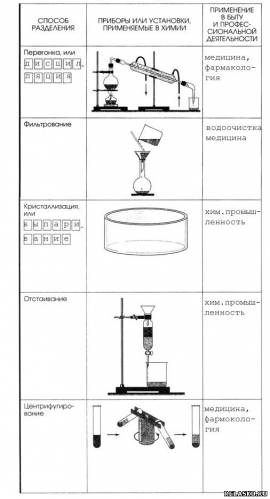
3. Заполните схему «Фильтрование воздуха в профессиональной деятельности человека».

4. Заполните схему «Фильтрование воды в быту и на производстве».

|
| |
| |
| Alicerok | | Сообщение # 50 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Назовите физические свойства веществ, на которых основаны способы разделения смесей:
1) дистилляция – разная температура кипения;
2) кристаллизация – разные размеры частиц;
3) возгонка – переход из одного агрегатного состояния в другое, минуя третье;
4) отстаивание – различная плотность;
5) фильтрование – разная пропускная способность пористого материала.
2. В сахар попали мелкие кусочки стекла. Как очистить сахар от опасных примесей? Выберите порядок действий.

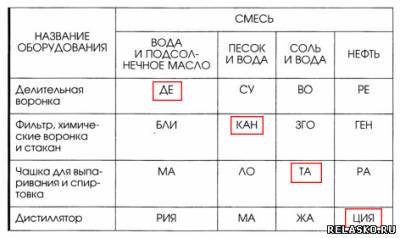
3. Установите соответствие между смесью и оборудованием, которое необходимо для её разделения. Из слогов, указывающих правильный ответ, вы составите слово, обозначающее осторожное сливание жидкости при образовании осадка на дне сосуда: декантация.
4. Предложите последовательность операций для разделения следующей смеси веществ:
песок, соль, железная стружка, сера.

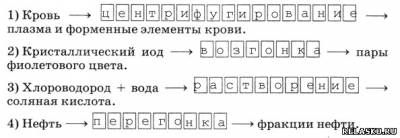
5. Впишите пропущенные слова в схемы получения различных веществ.
6. Подготовьте небольшое сообщение об одной из фракций нефти (название, физические свойства, области применения). Используйте дополнительные источники информации, в том числе Интернет.
Нефть разделяется на фракции в ректификационной колонке. Это стальной цилиндрический аппарат высотой 40 м. Она внутри имеет несколько десятков горизонтальных перегородок, т. е. тарелок.
Пары нефти, поступая в колонну, поднимаются вверх и проходят через отверстия в тарелках. При движении вверх они охлаждаются и сжижаются. Бензин образуется почти на самом верху, это
летучая, горючая жидкость, является углеводородом. Используется как топливо. Не смешивается с водой. В конце XIX века единственным способом применения бензина было использование его в качестве антисептического средства и топлива для примусов. В основном из нефти отгоняли только керосин, а все остальное утилизировали. После появления двигателя внутреннего сгорания бензин стал одним из главных продуктов нефтепереработки. Однако по мере распространения дизельных двигателей на первый план стало выходить дизельное топливо, благодаря более высокому КПД.
Бензин применяется как топливо для карбюраторных и инжекторных двигателей, высокоимпульсное ракетное топливо, при производстве парафина, как растворитель, как горючий материал, сырье для нефтехимии.
7. Используя Интернет, познакомьтесь с системой очистки воды, поступающей в водопроводную систему города. Укажите последовательность основных операций этого процесса в виде схемы.
1) Вода из реки поступает в бассейн для отстаивания – отстойник.
2) Оттуда поступает в колодец.
3) Проходит через грубый фильтр – слой песка для задержки крупных частиц.
4) Через главный насос вода поступает в устройство для хлорирования воды, для того, чтобы уничтожить вредные микроорганизмы.
5) Далее, вода поступает в водонапорную башню.
6) Следующая стадия – поступление через водопровод в город.
8. Укажите, в какой последовательности происходит испарение основных компонентов жидкой воздушной смеси. Приведите названия и формулы веществ.
1) Азот выкипает первым (N2)
2) Кислород (О2)
3) Углекислый газ (СО2).
|
| |
| |
| Alicerok | | Сообщение # 51 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 26. Химические реакции.
Часть I
1. Химические явления, или химические реакции, - это явления, при которых происходит превращения одних веществ в другие.
2. Образование новых веществ сопровождается появлением новых признаков или свойств, характеризующих эти вещества, что можно зафиксировать с помощью органов чувств, т.е. заметить признаки химических реакций.
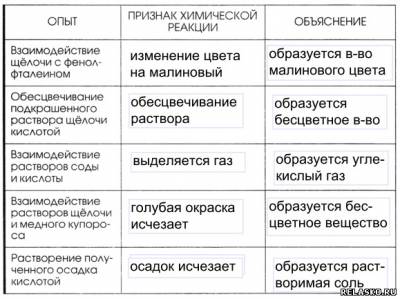
3. Заполните таблицу «Признаки химических реакций».
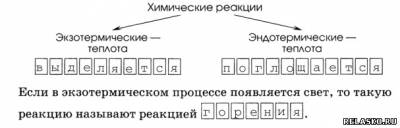
4. Классификация реакций по признаку выделения или поглощения теплоты.
5. Условия течения химических реакций:
- соприкосновение реагирующих веществ;
- первоначальное нагревание для некоторых экзотермических реакций;
- постоянное нагревание для эндотермических реакций.
|
| |
| |
| Alicerok | | Сообщение # 52 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. В каком случае можно говорить, что протекает химическая реакция?
1) В пробирку с раствором щёлочи приливают индикатор фенолфталеин.
3) В пробирку с раствором щёлочи приливают индикатор метиловый оранжевый.
Ответ поясните.
Так как в этих случаях наблюдается изменение окраски раствора, в 1 – раствор станет малиновый, во 3 – жёлтый.
2. Прочитайте внимательно стихотворение.
Явил ряд признаков подряд
Нам, разлагаясь, бихромат:
Цвет, звук, огонь и даже газ
Заметить каждый мог из нас.
Чтоб превращенье началось,
Поджечь кристаллы нам пришлось.
Тепло наружу – это экзо,
Горенье – свет,
Тепло вовнутрь – это эндо –
Обратный тепловой эффект!
О каких признаках описанной реакции говорится в стихотворении?
Изменение окраски, образование газа, появление запаха.
Если на уроке вам не демонстрировали эту реакцию, найдите в Интернете видеофрагмент «Разложение бихромата аммония», просмотрите его и сделайте рисунок, навеянный этой замечательной реакцией.
3. Установите соответствие между признаком и химической реакцией.

4. При приготовлении раствора серной кислоты следует:
2) серную кислоту приливать к воде.
Ответ поясните.
Выделяется большое количество теплоты, вода может закипеть и выбросить брызги на лицо и руки работающего.
5. Верны ли следующие суждения?
А. Экзотермические реакции, как правило, идут при постоянном нагревании.
Б. Эндометрические реакции могут протекать без нагревания.
4) оба суждения неверны.
6. Чтобы увеличить скорость химической реакции между твёрдыми и газообразными веществами, нужно измельчить твёрдое вещество.
7. Чтобы увеличить скорость химической реакции между твёрдыми растворимыми веществами, нужно измельчить и растворить их в воде.
8. Укажите, что нужно сделать, чтобы ликвидировать возгорание:
1) твёрдых веществ и материалов – закрыть плотным материалом;
2) нефтепродуктов – использовать огнетушитель;
3) электроприборов – обесточить и накрыть плотным материалом.
|
| |
| |
| Alicerok | | Сообщение # 53 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 27. Химические уравнения.
Часть I
1. Закон Ломоносова-Лавуазье – закон сохранения массы веществ:
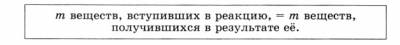
2. Уравнения химической реакции – это условная запись химической реакции с помощью химических формул и математических знаков.
3. Химическое уравнение должно соответствовать закону сохранения массы веществ, что достигается расстановкой коэффициентов в уравнении реакции.
4. Что показывает химическое уравнение?
1) Какие вещества вступают в реакцию.
2) Какие вещества образуются в результате.
3) Количественные отношения веществ в реакции, т. е. количества реагирующих и образующихся веществ в реакции.
4) Тип химической реакции.
5. Правила расстановки коэффициентов в схеме химической реакции на примере взаимодействия гидроксида бария и фосфорной кислоты с образованием фосфата бария и воды.
а) Запишите схему реакции, т. е. формулы реагирующих и образующихся веществ:
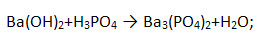
б) начинайте уравнивать схему реакции с формулы соли (если она имеется). При этом помните, что несколько сложных ионов в составе основания или соли обозначаются скобками, а их число – индексами за скобками:
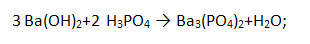
в) водород уравняйте в предпоследнюю очередь:
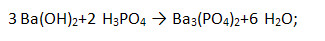
г) кислород уравняйте последним – это индикатор верной расстановки коэффициентов.
Перед формулой простого вещества возможна запись дробного коэффициента, после чего уравнение необходимо переписать с удвоенными коэффициентами.
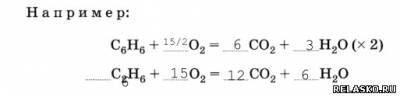
|
| |
| |
| Alicerok | | Сообщение # 54 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Составьте уравнения реакций, схемы которых:
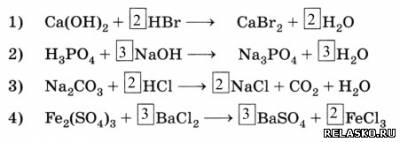
2. Напишите уравнения химических реакций:

3. Установите соответствие между схемой и суммой коэффициентов в химической реакции.

4. Установите соответствие между исходными веществами и продуктами реакции.

5. Что показывает уравнение следующей химической реакции:
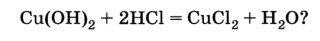
1) Вступили в реакцию гидроксид меди и соляная кислота;
2) Образовались в результате реакции соль и вода;
3) Коэффициенты перед исходными веществами 1 и 2.
6. С помощью следующей схемы составьте уравнение химической реакции, используя удвоение дробного коэффициента:
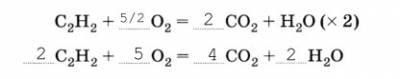
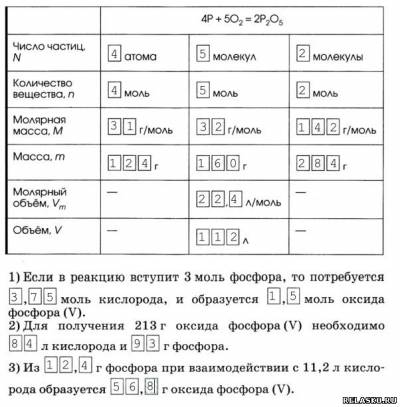
7. Уравнение химической реакции:
4P+5O2=2P2O5
показывает количество вещества исходных веществ и продуктов, их массу или объём:
1) фосфора – 4 моль или 124 г;
2) оксида фосфора (V) – 2 моль, 284 г;
3) кислорода – 5 моль или 160 л.
|
| |
| |
| Alicerok | | Сообщение # 55 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 28. Расчёты по химическим уравнениям.
Часть 1
1.
2. Рассмотрим пример.
Рассчитайте массу серной кислоты, которая взаимодействует с 5,6 г гидроксида калия. В результате реакции образуется сульфат калия и вода.

|
| |
| |
| Alicerok | | Сообщение # 56 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Заполните пропуски, проанализировав уравнение реакции.
2. Рассчитайте массу магния, который может сгореть в кислороде объёмом 33,6 л (н. у.). Схема химической реакции:

3. В реакцию вступили 13 г цинка и соляная кислота. В результате реакции образовались водород и хлорид цинка. Определите объём (н. у.) и число молекул водорода.

4. Навеска 1,12 г железа полностью «растворилась» в растворе сульфата меди (II). Вычислите массу образовавшегося осадка меди. Какое количество вещества сульфата железа (II) получилось при этом?

5. Вычислите массу гидроксида меди (II), который образуется при взаимодействии 200 г 20%-го раствора гидроксида натрия и избытка раствора сульфата меди (II). В результате реакции образуется также сульфат натрия.

6. Определите объём азота N2, необходимого для взаимодействия с кислородом, если в результате реакции получается 250 мл оксида азота (II).

7. Какой объём воздуха потребуется для взаимодействия 17,5 г лития, содержащего 20% примесей? В результате реакции получается оксид лития.

8. Придумайте задачу, при решении которой необходимо использовать следующую схему реакции:

Запишите условие задачи и решите её.
При взаимодействии 2 моль серной кислоты с нитратом свинца, образовался осадок, найти его массу.

|
| |
| |
| Alicerok | | Сообщение # 57 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 29. Реакции разложения.
Часть I
1. Признаки реакций разложения:
- в реакцию вступает одно сложное вещество;
- в результате реакции образуются два и более новых простых или сложных веществ;
- почти все эти реакции по тепловому эффекту эндотермические.
2. Интенсивность протекания реакций характеризует её скорость.
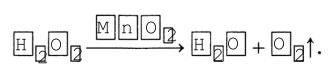
3. Вещества, изменяющие скорость реакции, называются катализаторами, а реакции с их участием – каталитическими. Например, разложение пероксида водорода в присутствии катализатора:
4. Биологические катализаторы белковой природы называются ферментами, а реакции с их участием – ферментативными. Например, разложение пероксида водорода в присутствии фермента:

|
| |
| |
| Alicerok | | Сообщение # 58 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Напишите уравнения химических реакций по описанию. Допишите, где необходимо, условия проведения реакций.

2. Расставьте коэффициенты в схемах химических реакций.
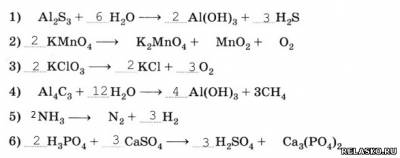
Какие реакции относятся к реакциям разложения?
2,3,4
3. Верны ли следующие суждения?
А. Почти все реакции разложения эндотермические.
Б. Катализаторы ускоряют химические реакции, но сами при этом не расходуются.
1) оба суждения верны.
4. Проведите домашний эксперимент.
1) Возьмите сырую и варёную картофелины.
2) Аккуратно порежьте их на мелкие кусочки.
3) Добавьте по отдельности перекись водорода к сырому и варёному картофелю.
Что наблюдаете?
При действии на сырую картошку выделяется кислород.
Объясните результаты опыта.
В сырой картошке крахмал взаимодействует с перекисью.
Какой газ выделяется? Как это можно доказать?
Кислород поддерживает горение.
5. С помощью Интернета и других источников информации найдите интересный факт применения катализатора или фермента в быту или на производстве. Опишите его.
Ферменты кисломолочных бактерий.
Способность молока со временем прокисать при комнатной температуре объясняется работой молочнокислых бактерий. Они поступают в молоко либо при контакте во время доения, либо из воздуха. В качестве источника энергии для собственного обмена веществ они используют молочный сахар - лактозу, превращая ее в молочную кислоту. Для ускорения этого процесса и его направления в нужное русло (чтобы молоко не стало горьким или же слишком кислым) молочнокислые бактерии добавляются при производстве сыра целенаправленно.
В самом простом случае, например, при производстве творога, в молоко добавляют немного созревших молочнокислых бактерий из уже сквашенных продуктов и немного подогревают. Это могут быть простокваша или йогурт, 1-2 ст. л. которых на литр молока достаточно для того, чтобы бактерии сразу же начали свою работу. Эти добавленные микроорганизмы, которые своими ферментами приводят в действие процесс созревания молока, называют исходными культурами. Они оказывают влияние на вкус, внешний вид и консистенцию готового сыра
6. Рассчитайте массу воды, которую необходимо разложить в электролизёре для получения 89,6 л кислорода

7. В лаборатории необходимо заполнить банку объёмом 1,5 л кислородом. Можно ли это сделать, если имеется всего 15,8 г KMnO4?

|
| |
| |
| Alicerok | | Сообщение # 59 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 30. Реакции соединения.
Часть I
1. Реакции соединения – это «химический антоним» реакции разложения.
2. Запишите признаки реакции соединения:
- в реакции участвуют 2 простых или сложных вещества;
- образуется одно сложное;
- выделяется тепло.
3. На основании выделенных признаков дайте определение реакций соединения.
Реакции соединения – это реакции, в результате которых образуется из одного или нескольких простых или сложных веществ одно сложное.
4. 
5.
По направлению протекания реакции делят на:
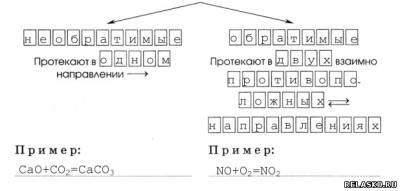
|
| |
| |
| Alicerok | | Сообщение # 60 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Запишите уравнения химических реакций:

2. Напишите уравнения химических реакций между хлором:
1) и натрием 2Na+Cl2=2NaCl
2) и кальцием Ca+Cl2=CaCl2
3) и железом с образованием хлорида железа (III) 2Fe+3Cl2=2FeCl3
3. Дайте характеристику реакции

4. Дайте характеристику реакции

5. Запишите уравнения реакций соединения, протекающих согласно схемам:
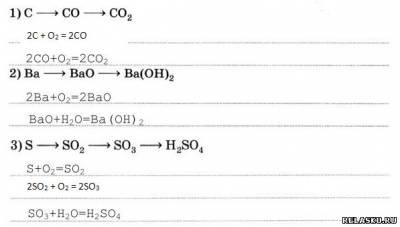
6. Расставьте коэффициенты в уравнениях реакций, схемы которых:
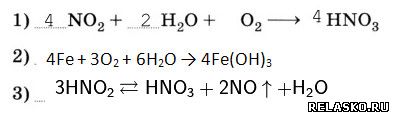
7. Верны ли следующие суждения?
А. Большинство реакций соединения являются экзотермическими.
Б. При повышении температуры скорость химической реакции увеличивается.
1) оба суждения верны
8. Рассчитайте объём водорода и массу серы, которые необходимы для образования 85 г сероводорода.

Смотреть решебник далее...
|
| |
| |