|
Решебник по Химии. 8 класс. Габриелян. Рабочая тетрадь
|
|
| Alicerok | | Сообщение # 76 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
|
Часть II
1. Гидроксид натрия взаимодействует со следующими из перечисленных веществ:
сульфат меди (II), хлорид магния, оксид меди (II), оксид серы (IV), сульфат калия, азотная кислота, хлорид аммония.
Ответ запишите формулами.
Ответ. CuSO4, MgCl2, SO2, HNO3, NH4Cl
Составьте возможные молекулярные и ионные уравнения реакций.
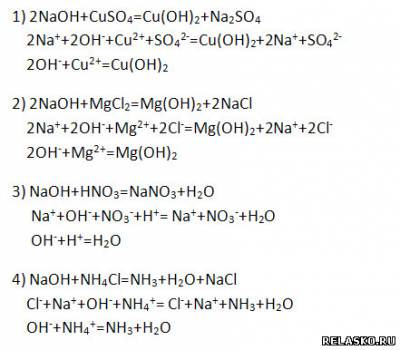
2. Приведите не менее трёх молекулярных уравнений с участием щёлочи, соответствующих следующему сокращённому ионному:
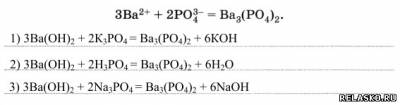
3. Приведите не менее трёх молекулярных уравнений, соответствующих следующему сокращённому ионному:
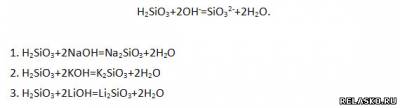
4. Приведите не менее трёх молекулярных уравнений, соответствующих следующему сокращённому ионному:
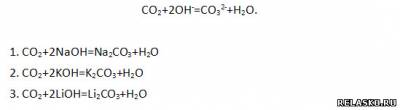
5. Определите неизвестные вещества и запишите молекулярные и ионные уравнения реакций, протекающих согласно схеме:

6. Вычислите массу (г) 10%-го раствора гидроксида кальция, необходимого для взаимодействия с 67,2 л углекислого газа (н. у.). Сколько граммов осадка образуется?

Сообщение отредактировал Alicerok - Среда, 07.10.2015, 12:46 |
| |
| |
| Alicerok | | Сообщение # 77 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 39. Соли, их классификация и химические свойства в свете ТЭД.
Часть I
1. Соли – это электролиты, которые при диссоциации в качестве катионов образуют катионы металла, кроме аммония, в качестве анионов – анионы кислотного остатка.
2.Классификация солей
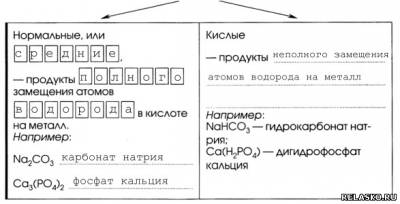
3. Химические свойства солей.

|
| |
| |
| Alicerok | | Сообщение # 78 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Запишите формулы следующих солей:

2. Распределите соли из задания 1 по двум группам.
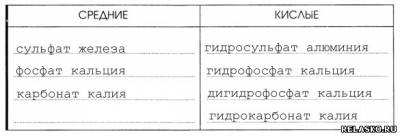
3. Сульфат железа (II) не может быть получен при взаимодействии:
3) железа с раствором сульфата магния.
Запишите молекулярные и ионные уравнения реакций, с помощью которых можно получить сульфат железа (II):

4. Веществами, при взаимодействии которых образуется соль, являются:
3) кислотный оксид и щёлочь.
Запишите пример уравнения возможной реакции.
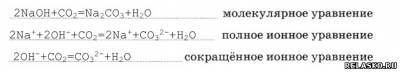
5. Запишите уравнения реакций, подтверждающих ионный состав хлорида кальция:

6. Запишите по одному уравнению реакций замещения, соединения и обмена, с помощью которых можно получить сульфат магния, в молекулярной и ионной формах:
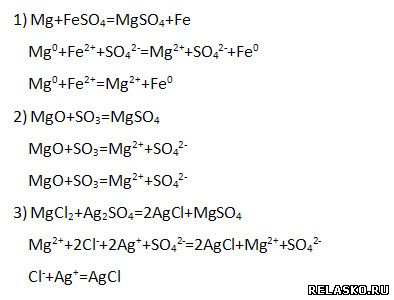
7. Составьте три молекулярных уравнения реакций между солями, соответствующих следующему сокращённому ионному:

8. Вычислите, сколько граммов 10% -х растворов исходных солей потребуется для получения 75 г карбоната кальция.

|
| |
| |
| Alicerok | | Сообщение # 79 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 40. Генетическая связь между классами неорганических соединений.
Часть I
1. Генетическая связь — это связь между веществами разных классов, основанная на их взаимопревращениях и отражающая единство их происхождения, т. е. генезис веществ.
2. Генетический ряд металла объединяет:
— один и тот же элемент-металл;
— вещества разных классов, образованные этим металлом;
— взаимопревращения веществ ряда.
Например:

3. Генетический ряд неметалла объединяет:
- кислотные оксиды
- кислоты
- соли
Например:

|
| |
| |
| Alicerok | | Сообщение # 80 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1.

2.

3.

4. К раствору гидроксида натрия добавили неизвестный раствор голубого цвета. Выпал студенистый осадок ярко-синего цвета. При нагревании последнего цвет изменился на чёрный. К полученной смеси прилили раствор серной кислоты. При нагревании исследуемой смеси образовался прозрачный раствор исходного голубого цвета. Запишите уравнения превращений в молекулярной и ионной формах.
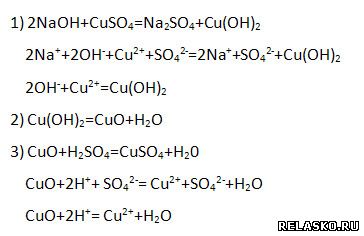
5. Вычислите массу осадка, который выпадает при сливании 807 г 20% -го раствора нитрата свинца с раствором, содержащим необходимое количество иодида калия. Определите количество иодида калия.

|
| |
| |
| Alicerok | | Сообщение # 81 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 41. Окислительно-восстановительные реакции (ОВР).
Часть I
1. ОВР — это реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вещества.
2. Восстановитель — это элемент или вещество, отдающее электроны. Само оно при этом окисляется.
Окислитель – это элемент или вещество, принимающее электроны. Само оно при этом восстанавливается.

3. Некоторые активные окислители:
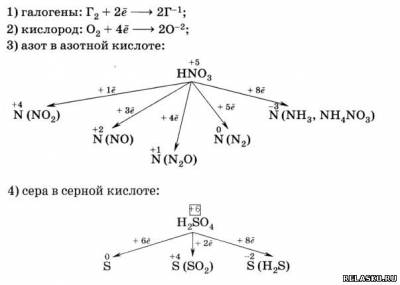
4. Некоторые активные восстановители:
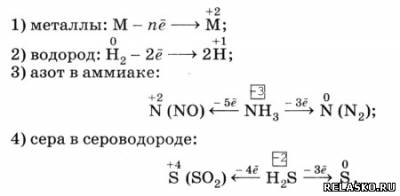
|
| |
| |
| Alicerok | | Сообщение # 82 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Самым сильным восстановителем среди элементов IVA группы является:
4) свинец
Обоснуйте свой выбор.
Т. к. восстановительные свойства в группе сверху вниз усиливаются, то в 4 группе самым сильным восстановителем будет свинец – он ниже всех остальных.
2. Наиболее слабым окислителем среди элементов VA группы является:
2) сурьма
Обоснуйте свой выбор.
Т. к. окислительные свойства элементов в группе сверху вниз ослабевают и ниже всех сурьма, то она будет самым слабым окислителем.
3. Окислительная активность галогенов возрастает от иода к фтору, потому что:
4) увеличивается их электроотрицательность
4. Максимальное значение степени окисления хлор проявляет в соединении, формула которого:
3) Сl2O7
5. Наименьшую степень окисления сера проявляет:
3) в сульфиде калия
6. Наименьшую степень окисления хром имеет в соединении:
1) Сг203
7. Окислительно-восстановительная реакция возможна между:
4) CuO и C
Запишите уравнение ОВР и составьте электронный баланс.

8. Сера проявляет восстановительные свойства в реакции, схема которой:

9. Рассмотрите взаимодействие алюминия с соляной кислотой:

10. Верны ли следующие суждения?
А. Сероводород проявляет только восстановительные свойства.
Б. Серная кислота проявляет как окислительные, так и восстановительные свойства.
2) верно только А
Обоснуйте свой ответ.
Сероводород (H2S) не может быть окислителем, т. к. сера в данном соединении имеет минимальную степень окисления -2, ее внешний энергетический уровень полностью заполнен электронами, т. е. она уже больше не в состоянии принимать электроны, она может только отдавать их (проявляет только восстановительные свойства) .
H2SO4 не может быть восстановителем, т. к. сера в данном соединении имеет максимальную степень окисления +6, на внешнем энергетическом уровне нет ни одного электрона, т. е. она может только принимать электроны, но не отдавать их (проявляет только окислительные свойства).
|
| |
| |
| Jumerra | | Сообщение # 83 |
|
Группа: Пользователи
Сообщений: 1
Статус: Offline
| Как бы странно этот вопрос не звучал,но какое у вас любимое соединение железа
Например мне нравится как Fe взаимодействует с солями
Соли Fe (+3): FeCl3, Fe2(SO4)3
Растворы солей трехвалентного железа имеют желтый окрас и являются слабыми окислителями.
При воздействии восстановителей переходят в те вещества, где железо имеет степень окисления +2.
Важно!
Солей данного типа открыто достаточно много, и все они используются в промышленных, медицинских отраслях, а также в повседневной жизни.
Источник: https://nauka.club/ximiya....mi.html
|
| |
| |