|
Решебник по Химии. 8 класс. Габриелян. Рабочая тетрадь
|
|
| Alicerok | | Сообщение # 1 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Решебник и ГДЗ по Химии. 8 класс. О. С. Габриелян, С. А. Сладков. Рабочая тетрадь

Авторы: О. С. Габриелян, С. А. Сладков
Учебник с задачами, примерами и ответами по ФГОС 2007, 2008, 2009, 2010, 2011, 2012, 2013, 2014 год
Данный решебник и готовые домашние задания по Химии предназначены для учителей и учеников 8 класса средней школы для проверки своих знаний предмета, а также для помощи в решении домашних заданий.
Преподаватели урока Химии с помощью данного учебника смогут легко и быстро проверять ответы на домашние работы у своих учеников, а так же подготовиться к уроку.
Родители учеников могут так же проверять своих детей, на сколько правильно они сделали домашнюю работу.
Оглавление решебника и ГДЗ по Химии. 8 класс. О. С. Габриелян, С. А. Сладков. Рабочая тетрадь
Тема 1. Предмет химии. Вещества.
Тема 2. Превращения веществ. Роль химии в жизни человека. История развития химии.
Тема 3. Периодическая система химических элементов Д. И. Менделеева. Знаки химических элементов.
Тема 4. Химические формулы. Относительные атомная и молекулярная массы.
Тема 5. Атомы химических элементов. Основные сведения о строении атомов. Изотопы.
Тема 6. Строение электронных оболочек атомов.
Тема 7. Изменение свойств элементов в периодах и группах.
Тема 8. Ионная химическая связь.
Тема 9. Ковалентная химическая связь.
Тема 10. Ковалентная полярная химическая связь.
Тема 11. Металлическая химическая связь. Обобщение знаний о типах химической связи.
Тема 12. Простые вещества. Простые вещества — металлы.
Тема 13. Простые вещества — неметаллы.
Тема 14. Количество вещества. Молярная масса.
Тема 15. Молярный объём газов.
Тема 16. Основные и производные единицы измерения количества, массы и объёма веществ.
Тема 17. Соединения химических элементов. Степень окисления.
Тема 18. Оксиды и летучие водородные соединения.
Тема 19. Основания.
Тема 20. Кислоты.
Тема 21. Соли.
Тема 22. Кристаллические решётки.
Тема 23. Чистые вещества и смеси.
Тема 24. Массовая и объёмная доли компонентов смеси.
Тема 25. Изменения, происходящие с веществами.
Тема 26. Химические реакции.
Тема 27. Химические уравнения.
Тема 28. Расчёты по химическим уравнениям.
Тема 29. Реакции разложения.
Тема 30. Реакции соединения.
Тема 31. Реакции замещения.
Тема 32. Реакции обмена.
Тема 33. Типы химических реакций на примере свойств воды.
Тема 34. Растворы. Растворение.
Тема 35. Основные положения теории электролитической диссоциации (ТЭД).
Тема 36. Оксиды, их классификация и химические свойства.
Тема 37. Кислоты, их классификация и химические свойства в свете ТЭД.
Тема 38. Основания, их классификация и химические свойства в свете ТЭД.
Тема 39. Соли, их классификация и химические свойства в свете ТЭД.
Тема 40. Генетическая связь между классами неорганических соединений.
Тема 41. Окислительно-восстановительные реакции (ОВР).
Сообщение отредактировал Alicerok - Вторник, 06.10.2015, 14:35 |
| |
| |
| Alicerok | | Сообщение # 2 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 1. Предмет химии. Вещества.
Часть I
1. Химия изучает:
- вещества
- их строение
- их свойства
2. Вещество – это то, из чего сделаны физические тела.
3. Признаки, по которым одни вещества отличаются от других, - это свойства, например: водород – газ, лёгкий, без запаха, цвета, вкуса.
4. Существует взаимосвязь: свойство вещества – применение вещества.
Например, для стекла:
1) прозрачное – используют в качестве оконных стёкол
2) изготовление хрусталя
3) витражное стекло
5. Вещества состоят из молекул, которые, в свою очередь, образованы из атомов. Определённый вид атомов называют химическим элементом. Всего известно 119 химических элементов.
6. Химический элемент существует в трёх формах.
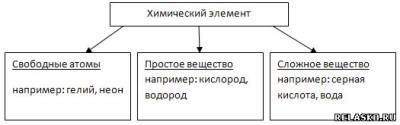
Простые вещества – это вещества, образованные атомами одного и того же химического элемента.
Вещества, образованные из двух и более химических элементов, называются сложными.
|
| |
| |
| Alicerok | | Сообщение # 3 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Установите соответствие между понятием и примером.

Ответ: А – 1, 3, 5
Б – 2, 4, 6
2. Вычеркните «лишнее»:
Колба, пробирка, химический стакан, мензурка, ступка, мерный цилиндр, кристаллизатор.
Укажите признак, общий для оставшихся объектов.
- Химическая посуда, сделанная из стекла.
3. Составьте задание, аналогичное предыдущему.
Вычеркнуть лишнее: пипетка, пробирка, резиновая груша, фильтровальная бумага, мерная колба, мензурка.
4. Заполните таблицу «Физические свойства веществ». В качестве примеров опишите вещества, используемые на кухне.
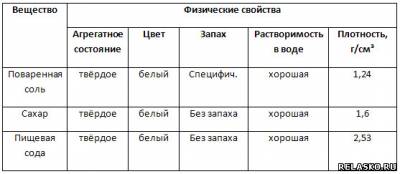
5. Укажите прилагательные, которые характеризуют свойства воды.
1) жидкая
3) бесцветная
4) прозрачная
6. Заполните таблицу «Сравнение физических свойств газообразных веществ».
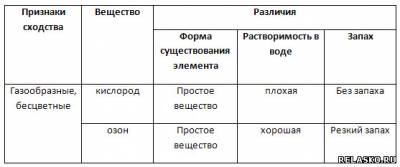
7. Заполните таблицу «Сравнение физических свойств меди и железа».
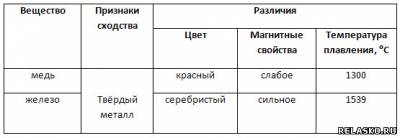
8. Составьте кроссворд о свойствах и применении какого-либо вещества (по своему выбору).
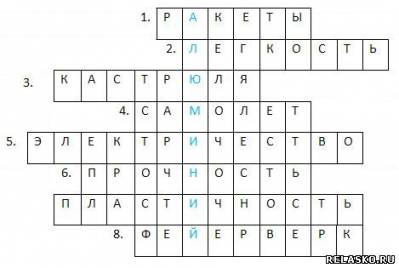
1. Аппарат, при производстве которого используются сплавы алюминия.
2. Физическое свойство алюминия, которое позволяет использовать его сплавы в самолетостроении.
3. Емкость для приготовления пищи методом варки, сделанная из алюминия.
4. Воздушное судно, предназначенное для полетов в атмосфере, при производстве которого используются сплавы алюминия.
5. Благодаря теплопроводности и способности проводить это, алюминий используется для изготовления электрических проводов.
6. Физическое свойство алюминия, которое наряду с легкостью, позволяет использовать его сплавы в ракето- и самолетостроении.
7. Это физическое свойство металла позволяет делать из алюминия фольгу.
8. Свойство алюминия гореть ослепительным пламенем применяется для получения этих декоративных праздничных огней.
9. На примере химического элемента водорода укажите правильную последовательность (1-2-3) перечисленных понятий от единичного к общему. Конкретизируйте её, используя слова и рисунки моделей частиц.
3) Вещество – это то, из чего состоят физические тела.
1) Атом – это химически неделимая частица.
2) Молекула – это наименьшая частица вещества, обладающая его свойствами.
10. Выражения, являющиеся синонимами понятия «химический элемент».
1) вид одинаковых атомов
3) вид атомов, имеющих одинаковые свойства.
11. Установите соответствие между формой существования химического элемента и рисунками моделей частиц.
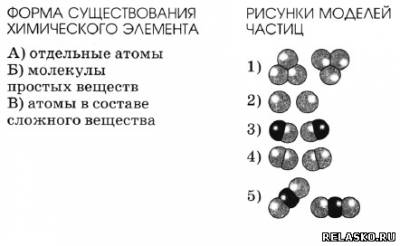
Ответ: А-2; Б-1, 4; В-3, 5.
12. Проанализируйте рисунки и впишите пропущенные слова.
На рисунках изображено две молекулы сложных веществ, образованных из двух химических элементов.
13. Отметьте фразы, в которых говорится о сере как о химическом элементе. Из букв, соответствующих правильным ответам, вы составите название химического элемента, соединения которого используют для обеззараживания воды: хлор.
2) сера входит в состав молекул серной кислоты Х
3) некоторые белки содержат серу Л
5) молекулы сероводорода образованы серой и водородом О
7) молекулы серы состоят из 8 атомов Р
В тех фразах, которые вы не выбрали, речь идёт о сере как о простом веществе.
|
| |
| |
| Alicerok | | Сообщение # 4 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 2. Превращения веществ. Роль химии в жизни человека. История развития химии.
Часть I
1. Изменения, происходящие с телами и веществами, - это
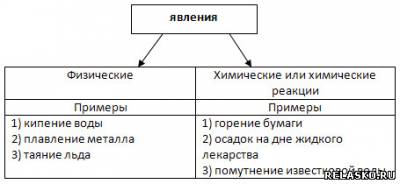
2. Отношение людей к химии.
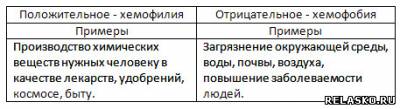
3. Артефакт алхимии – философский камень.
Он (укажите роль):
1) смешивание эликсиров
2) целительство, врачевание
4. Заполните таблицу «Великие русские химики».

|
| |
| |
| Alicerok | | Сообщение # 5 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Выберите синонимы понятия «химические явления».
2) химические реакции
3) явления, при которых из одних веществ образуются другие вещества
4) явления, при которых изменяется цвет вещества, образуется осадок или газ
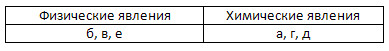
2. Разделите явления на физические (А) и химические (Б).
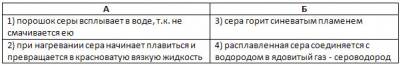
3. Проанализируйте рисунки и назовите процесс.
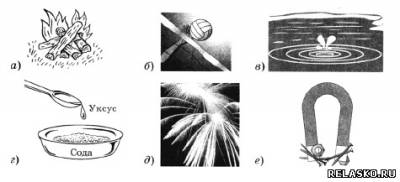
а) горение – химическое явление
б) подача мяча – физическое явление
в) растворение – физическое явление
г) гашение соды – химическое явление
д) горение - химическое явление
е) притягивание магнитом - физическое явление
Установите соответствие между физическим или химическим явлением и процессом, изображённым на рисунке.
4. Сделайте презентацию на одну из предложенных тем: «Отрицательное значение химии» или «Положительное значение химии», используя возможности Интернета.
5. Вычеркните «лишнее»:
Замерзание воды, испарение воды, кипение воды, разложение воды на водород и кислород, фильтрование воды.
6. Заполните таблицу «Физические и химические явления», используя результаты своих наблюдений за процессами в быту и в природе.

7. С помощью Интернета и других источников информации (научная литература) сделайте сообщение о жизни и творчестве одного из трёх великих русских химиков по следующему плану:
1) детство;
2) учёба в юношеские годы;
3) научная деятельность, основные научные достижения.
Д. И. Менделеев – родился в семье директора попечителя училищ, был 14 и самым любимым ребёнком в семье. Воспитывала его мать, так как отец вскоре после его рождения ослеп и умер.
Менделеев в гимназии не отличался особым прилежанием, особенно не любил закон Божий. Он хотел поступить в медицинскую академию,
но биология оказалась ему не под силу, и пошёл в педагогику.
Учился он хорошо, но сильно заболел, и посоветовали лекари ему поехать на юг. Вылечился, блестяще защитился и начал исследовательские работы.
1. Исследовал явление изоморфизма.
2. Сконструировал пикнометр – прибор для определения плотности жидкостей.
3. Открыл температуру кипения жидкостей, их критическую температуру.
4. Издал первый учебник по органической химии в России.
5. Создал гидратную теорию растворов.
6. Открыл периодическую систему химических элементов, сформулировал Периодический закон.
7. На основе закона и таблицы предсказал существование нескольких химических элементов.
|
| |
| |
| Alicerok | | Сообщение # 6 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 3. Периодическая система химических элементов Д. И. Менделеева. Знаки химических элементов.
Часть I
1. По горизонтали таблица Д. И. Менделеева делится на периоды, которые подразделяются на:
а) малые, это периоды – 1, 2, 3;
б) большие, это периоды – 4, 5, 6, 7.
2. По вертикали таблица Д. И. Менделеева делится на группы, каждая из которых подразделяется на:
а) главную, или А группу;
б) побочную, или В группу.
IА группа – это группа щелочных металлов.
IIА группа – это группа щелочноземельных металлов.
VIIА группа – это группа галогенов.
VIIIА группа – это группа благородных, или инертных газов.
4. Аналогии языка химии с русским языком.
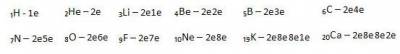
5. Дополните таблицу «Названия и знаки химических элементов».
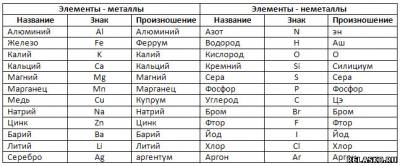
6. Примеры названий химических элементов (в скобках укажите химический знак) в соответствии с этимологическими источниками.
1) Свойства простых веществ
Водород (Н), кислород (О), фтор (F)
2) Астрономия
Селен (Se), теллур (Te), уран (U)
3) География
Германий (Ge), галлий (Ga), полоний (Po)
4) Древнегреческие мифы
Тантал (Та), прометий (Pm), лютеций (Lu)
5) Великие учёные
Менделевий (Md), резерфордий (Rt), эйнштейний (Es)
|
| |
| |
| Alicerok | | Сообщение # 7 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Установите соответствие между положением химического элемента в Периодической системе Д. И. Менделеева и химическим знаком.

А - 5; Б - 1; В – 2; Г – 4
2. Выберите символы или названия химических элементов одного большого периода. Из букв, соответствующих правильным ответам, вы составите название металла, который используется для изготовления бенгальских огней: магний.
1) калий М
2) Br А
5) марганец Г
6) Cu Н
8) Ca И
9)Zn Й
3. Впишите в соответствующие столбцы названия следующих химических элементов:
Cl, He, Br, Ne, Li, I, K, Ba, Ca, Na, Xe, Sr.
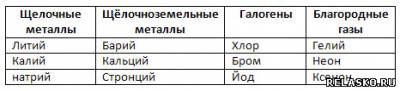
4. Заполните пропуски в логической схеме.
Химический элемент (Н, О) → химическая реакция (Н₂О) → химическое получение (2 Н₂О = 2 Н₂ + О₂).
5. Сделайте обобщение:
химические элементы – углерод, кремний, олово, свинец – относятся к IVА группе.
6. В левую колонку таблицы запишите, по какому признаку химические элементы разделены на две группы.

7. Установите соответствие между произношением и химическим знаком (символом).

А – 3; Б – 6; В – 2; Г – 7; Д – 5; Е – 1.
8. Вычеркните «лишнее»:
Кюрий, менделевий, бром, эйнштейний.
9. Общий этимологический источник названий химических элементов:
U, Te, Se – это планетарий.
10. В честь различных государств или частей света названы элементы:
Германий, галлий, франций, дубний
|
| |
| |
| Alicerok | | Сообщение # 8 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 4. Химические формулы. Относительные атомная и молекулярная массы.
Часть I
1.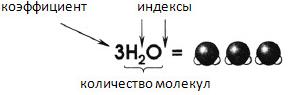
2. Ar элемента показывает, во сколько раз масса его атома больше 1/12 массы атома углерода.
Она указана в таблице Д. И. Менделеева, например:
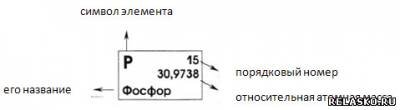
Ar (Н) = 1
Ar (О) = 16
Ar (N) = 14
Ar (Fe) = 56
Ar (Сu) = 64
Ar (Cl) = 35,5
3. Mr вещества показывает, во сколько раз масса молекулы данного вещества больше 1/12 массы атома углерода.
Mr равна сумме Ar элементов с учётом их индексов.
Mr (Н₂О) = 2*1+16=18
Mr (Н₂ SO₄) =2*1+32+4*16=98
Mr (CO₂) = 1*12+2*16=44
Mr [Ca₃(PO₄)] = 3*40+2*31+8*16=310
4. Заполните таблицу «Информация о веществе».
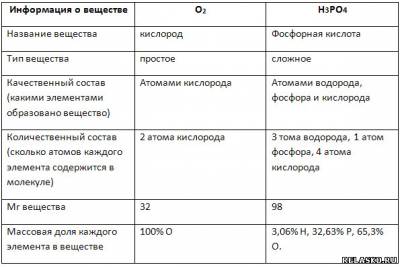
|
| |
| |
| Alicerok | | Сообщение # 9 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Установите соответствие между формулой вещества и составом молекулы вещества.

А – 4; Б – 6; В – 2; Г – 5.
2. Разделите указанные вещества на простые и сложные:
N₂, NO, O₃, AlCl₃, Na₂So₄, FeCl₂, Ca, Cl₂, KMnO₄, P₄.
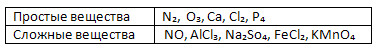
3. Исправьте неверно вычисленные значения относительных молекулярных масс для некоторых из приведённых формул.
3) Mr (AlCl₃) = 133,5
6) Mr (Al₂(SO₄)₃) = 342
4. Установите соответствие между записью и тем, что она обозначает.

А – 4; Б – 3; В – 1; Г – 2.
5. Молекула сахарозы состоит из 12 атомов углерода, 22 атомов водорода и 11 атомов кислорода. Напишите её формулу и рассчитайте относительную молекулярную массу.

8. Запишите формулы вещества, зная их произношение. Рассчитайте Mr.
1) N₂O, Mr (N₂O) = 2*14+16=44
2) H₂SiO₃, Mr (H₂SiO₃) = 2*1+28+3*16=78
3) CuSO₄, Mr (CuSO₄) = 64+32+4*16=160
9. Придумайте и решите задачу на расчёт массовой доли химического элемента в составе сложного вещества, состоящего из двух элементов.
Найти массовую долю каждого элемента в Na₂O.

|
| |
| |
| Alicerok | | Сообщение # 10 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 5. Атомы химических элементов. Основные сведения о строении атомов. Изотопы.
Часть I
1.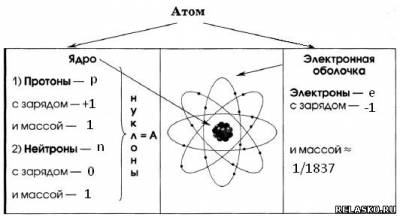
2. Вся масса атома сосредоточена в ядре. Число нейтронов N = A – Z, где Z – порядковый номер.
3. Порядковый номер элемента соответствует заряду атомного ядра, т.е. числу протонов в нём. Так как атом электронейтрален, то порядковый номер элемента также соответствует числу электронов.
4. Изменение числа протонов в ядре атома химического элемента приведёт к образованию атомов другого химического элемента. Следовательно, химический элемент – это совокупность атомов с одинаковым числом протонов.
5. Изменение числа нейтронов в ядре атома химического элемента приводит к образованию изотопов.
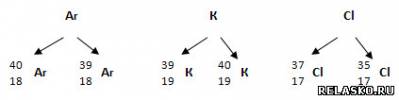
|
| |
| |
| Alicerok | | Сообщение # 11 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Выберите верные утверждения.
1) Ядро атома содержит протоны и нейтроны, суммарная масса которых равна массовому числу атома.
2) Нейтрон – это электронейтральная частица с массой, равной 1.
4) Электрон – это отрицательно заряженная частица с массой, равной 1.
2. Заполните таблицу «Состав атомов химических элементов».
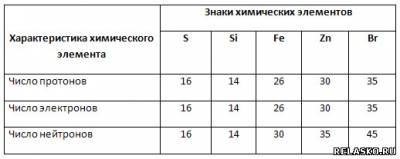
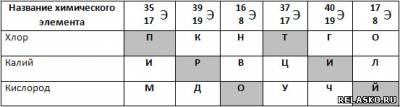
3. Установите соответствие между названием химического элемента и условными обозначениями его атомов. Из букв, соответствующих правильным ответам, вы составите название самого лёгкого из изотопов водорода:
протий.
4. Определите, в каких парах химических элементов число нейтронов в ядре атома одного из элементов вдвое больше.
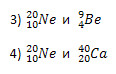
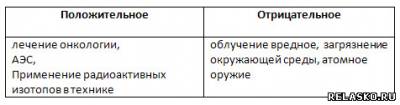
5. Приведите примеры использования явления радиоактивности, применения ядерных процессов, подчеркнув их положительное и отрицательное влияние на человека.
6. Запишите названия и символы химических элементов, в атомах которых:
1) 5 протонов, 6 нейтронов и 5 электронов - бор В;
2) 10 протонов, 10 нейтронов и 9 электронов – неон Ne;
3) 15 протонов, 15 электронов и 16 нейтронов - фосфор Р.
7. Установите соответствие между понятием и его определением.


Сообщение отредактировал Alicerok - Вторник, 06.10.2015, 15:37 |
| |
| |
| Alicerok | | Сообщение # 12 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 6. Строение электронных оболочек атомов.
Часть I
1. Совокупность электронов в атоме называется электронной оболочкой.
2. Электроны на электронной оболочке атома располагаются по электронным слоям, или энергетическим уровням.

3. Номер периода соответствует числу электронных слоёв в атоме химического элемента.
4. Номер группы соответствует числу электронов на внешнем энергетическом уровне.
5. Запишите схемы строения электронных оболочек атомов химических элементов с порядковыми номерами с 1-го по 10-й в таблице Д. И. Менделеева, а также калия и кальция.
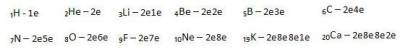
|
| |
| |
| Alicerok | | Сообщение # 13 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. В приведённом перечне: мышьяк, теллур, германий, йод, селен, полоний, астат, - число элементов, в атомах которых по шесть электронов на внешнем энергетическом уровне, равно:
3) трём.
2. Атомы химических элементов 4-го периода имеют одинаковое число:
3) энергетических уровней.
3. Установите соответствие между символом химического элемента (в заданном порядке) и числом электронов на внешнем энергетическом уровне его атома. Из букв, соответствующих правильным ответам, вы составите название установки, которая позволит человечеству ещё глубже познать строение атома: коллайдер.
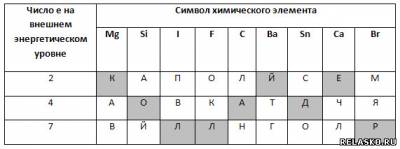
4. Установите соответствие между символом химического элемента (в заданном порядке) и числом энергетических уровней в электронной оболочке атома. Из букв, соответствующих правильным ответам, вы составите название частиц, из которых, в свою очередь, состоят протоны и нейтроны: кварки.
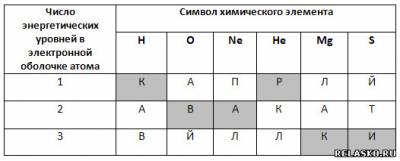
5. Верны ли следующие суждения?
А. Число электронов в электронной оболочке атома Cl равно 7.
Б. Число электронов на внешнем энергетическом уровне атома Br равно 35.
4) Оба суждения неверны.
6. Вычеркните «лишний» химический элемент из ряда
P, Be, S, N, Ne, Ca, H
По признаку завершённости внешнего электронного слоя атома.
7. Предложите алгоритм составления электронной схемы атома химического элемента.
1. Определить общее число электронов на оболочке по порядковому номеру;
2. Определить число энергетических уровней по номеру периода;
3. Определить число внешних электронов по номеру группы;
4. Рассчитать число электронов на предпоследнем уровне, предварительно указав число электронов на всех уровнях.
8. Сравните строение электронных оболочек атомов Ca и Mg.
1) сходство: на внешнем уровне есть одинаковое число электронов, равное 2
кальций 2е8е8е2е, магний 2е8е2е.
2) различие: в числе энергетических уровней, у кальция 4, у магния 3.
|
| |
| |
| Alicerok | | Сообщение # 14 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Тема 7. Изменение свойств элементов в периодах и группах.
Часть I
1.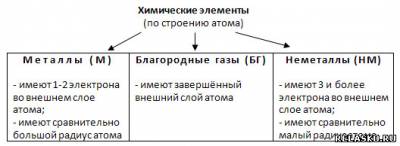
2. Металлы в стремлении получить завершённый внешний электронный слой атома отдают свои внешние электроны, а неметаллы принимают недостающие до 8 электроны.
3. В группе с ростом порядкового номера элементов усиливаются металлические свойства и ослабевают неметаллические, потому что:
1) увеличивается число энергетических уровней
2) постоянно число электронов на внешнем уровне
3) увеличивается радиус атома
4. В периоде с ростом порядкового номера элементов усиливаются неметаллические свойства и ослабевают металлические, потому что:
1) увеличивается число электронов на внешнем уровне
2) постоянно число уровней
3) увеличивается заряд атомных ядер
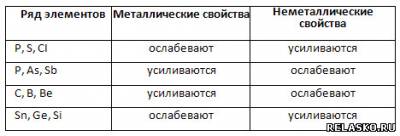
5. Заполните таблицу «Свойства химических элементов», указав усиление или ослабление свойств в ряду.
|
| |
| |
| Alicerok | | Сообщение # 15 |
|
Группа: Проверенные
Сообщений: 88
Статус: Offline
| Часть II
1. Выберите символы химических элементов-неметаллов. Из букв, соответствующих правильным ответам, вы составите название чрезвычайно токсичного газа бледно-жёлтого цве¬та с резким запахом: фтор.

2. Верны ли следующие суждения?
А. По периоду слева направо радиус атома увеличивается.
Б. По группе снизу вверх радиус атома уменьшается.
3) верно только Б.
3. Обведите знак «больше» или «меньше», если речь идёт о металлических свойствах в первом случае и о неметаллических — во втором.

4. Составьте кроссворд на тему «Благородные газы», используя Интернет.
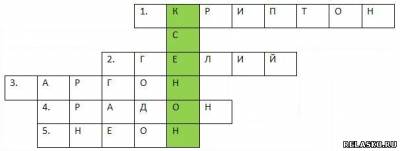
1. Этот инертный газ используют в энергосберегающих лампочках
2. Этим газом заполняют воздушный шары, он самый легкий среди инертных газов.
3. Этот инертный газ – третий по содержанию после азота и кислорода компонент воздуха, самый распространённый инертный газ в земной атмосфере.
4. При нормальных условиях — бесцветный инертный газ; радиоактивен, может представлять опасность для здоровья и жизни.
5. Трубки, заполненные смесью этого газа и азота, при пропускании через них электрического разряда дают красно-оранжевое свечение, в связи с чем они широко используются в рекламе.
6. По вертикали в цветных клетках вы получите название первого инертного газа, для которого были получены настоящие химические соединения.
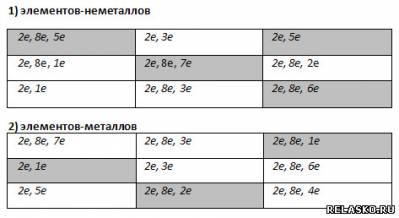
5. Поиграйте в «крестики-нолики». Покажите выигрышный путь, который составляют электронные схемы атомов:
6. Постройте график зависимости порядковых номеров химических элементов одного периода от радиусов их атомов, условно приняв изменение радиусов соседних элементов за 1. Сделайте вывод:
Радиусы атомов в пределах периодов с увеличением порядкового номера уменьшаются.
7. Постройте график зависимости порядковых номеров химических элементов одной группы от радиусов их атомов, условно приняв изменение радиусов соседних элементов за 1. Сделайте вывод:
В пределах группы радиусы атомов с увеличением порядкового номера увеличиваются.
Смотреть решебник далее...
|
| |
| |